מכונות מולקולריות: הדרך לאבחן ולרפא בו-זמנית
הוא מכין במעבדה חומרים חכמים שמחביאים בתוכם תרופות ומוביל שיטה פורצת דרך המשלבת אבחון וטיפול במולקולה אחת. הכירו את ד"ר עבד סעדי, כימאי אורגני שמכין במעבדה מולקולות מורכבות שלא היו קיימות בטבע מעולם, במטרה לרתום אותן לטובת המהפכה הבאה בעולם הרפואה.
תארו לעצמכם עולם שבו טיפול כימותרפי אינו כרוך עוד בנשירת שיער, בבחילות או בחולשה קיצונית – עולם שבו התרופה יודעת לנווט את דרכה בגוף כמו טיל מונחה, ולהשתחרר רק כשהיא מגיעה ליעדה הספציפי בלי להזיק בדרך. החזון הזה, שנראה בעבר כמעט בלתי אפשרי, הוא המנוע המדעי של ד"ר עבד סעדי - מרצה בכיר במחלקה לכימיה ובמכון לננו-טכנולוגיה (BINA) באוניברסיטת בר-אילן ואחד מהחוקרים הצעירים המובילים במרכז דנגור לרפואה מותאמת אישית.
המבנה שמאפשר למולקולה לנוע בחופשיות במערכת
בשנת 2016, ארבע שנים לפני שסעדי החל את הפוסט-דוקטורט שלו, הוענק פרס נובל לכימיה בתחום של תכנון וסינתזה של מכונות מולקולריות. אלה מולקולות קטנות, שתוכננו במעבדה כך שיוכלו לבצע תנועה מכנית נשלטת בתגובה לגירוי חיצוני כמו אור, חום או שינוי כימי. מאז, חוקרים ברחבי העולם החלו לחפש דרכים להשתמש במולקולות אלה בתחומים שונים.
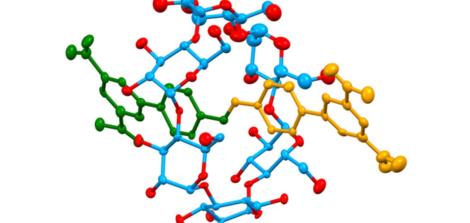
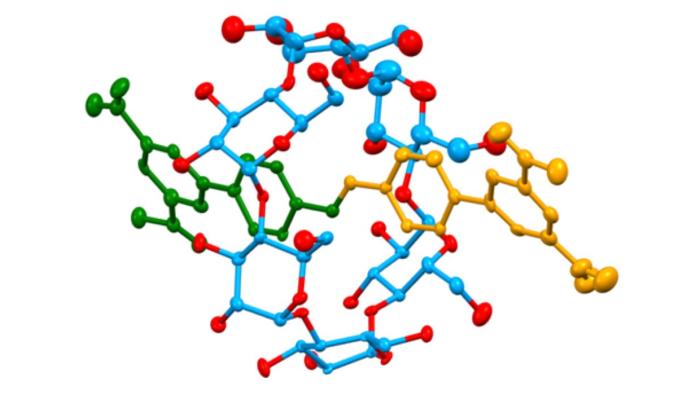
המבנה המרכזי שבו מתמחה ד"ר סעדי נקרא רוטקסן (Rotaxane) – חומרים שמחוברים על ידי קשר מכני ייחודי המאפשר להם לבצע פעולות כימיות וביולוגיות, כמו מכונה. כדי להבין איך המכונה הזו פועלת, נדמיין מזרק קטנטן שבו התרופה נמצאת בפנים, אך הבוכנה שלו נעולה. כדי שהתרופה תצא ותפעל, מישהו חייב להזיז את הנעילה בדיוק ברגע ובמקום הנכונים.
בשונה מקשר כימי רגיל, שהוא מעין דבק חזק המצמיד אטומים זה לזה במבנה קשיח, הרוטקסן מבוסס על קשר מכני. דמיינו טבעת המושחלת על מוט שבקצותיו יש מעין מעצורים המונעים ממנה לברוח. "זה כמו מפתח המושחל על טבעת בצרור מפתחות", מסביר ד"ר סעדי. "המפתח והטבעת לא מודבקים זה לזה – הם פשוט כלואים פיזית זה בתוך זה כמו חוליות בשרשרת. זה מה שמאפשר לטבעת 'לגלוש' על המוט בחופשיות מצד לצד מבלי להתנתק".
החופש המכני הזה הוא שהופך את המולקולה למכונה חכמה: הטבעת מתפקדת כמכסה או כבוכנה. ד"ר סעדי מהנדס את המולקולה כך שכאשר היא עוברת בזרם הדם, הטבעת ממוקמת בנקודה שחוסמת ומחביאה את התרופה תחתיה. במצב הזה, התרופה נותרת "רדומה" ואינה פוגעת בתאים בריאים.
איך נפתח המנעול? הסוד טמון בשימוש בטריגרים, גירויים ייחודיים לסביבת המחלה. ד"ר סעדי מתכנן את המכונה כך שהיא תגיב לתנאים הספציפיים הקיימים בגידול הסרטני כמו רמת חומציות או אנזימים יחודיים, בעוד בשאר הגוף המנעול נשאר סגור הרמטית.
כשהמכונה מגיעה ליעדה, הטבעת "מחליקה" בתגובה לחומציות או לאנזים, ומשחררת את התרופה החבויה. המזרק המולקולרי משחרר את המטען שלו אך ורק בתוך המטרה, וכך הופכת המולקולה ממבנה כימי סטטי למכונה דינמית שיודעת לקרוא את המפה של הגוף ולהגיב אליה.
 "במעבדה, האתגר הוא לייצר רק את הצורון ה'טוב' ולא את תמונת הראי שלו. היכולת לסנתז מכונה בעלת כיווניות ספציפית היא קריטית לבטיחות המטופל".
"במעבדה, האתגר הוא לייצר רק את הצורון ה'טוב' ולא את תמונת הראי שלו. היכולת לסנתז מכונה בעלת כיווניות ספציפית היא קריטית לבטיחות המטופל".
חיישן כימי: לראות את התרופה פועלת בזמן אמת
גולת הכותרת של מחקרו של ד"ר סעדי היא התרנוסטיקה (Theranostics) – תחום המשלב אבחון (דיאגנוסטיקה) וטיפול (תרפיה) במולקולה אחת. זוהי שיטה מתקדמת שבה הרוטקסן מתפקד כיחידה רב-תכליתית אשר נושאת עליה חיישן פלואורסצנטי או חומר ניגוד ל-MRI ויחד איתם היא מובילה את המטען התרופתי. "אנחנו מהנדסים את החומר כך שהוא 'יחביא' בתוכו את התרופה וימנע ממנה ליצור אינטראקציה עם רצפטורים בגוף בדרך ליעד", מסביר ד"ר סעדי כיצד מונעת ההמצאה הזו תופעות לוואי.
הרוטקסן מצויד בחיישן כימי רגיש המזהה תנאים הייחודיים לגידול סרטני, כמו רמת חומציות (pH) ספציפית או אנזים מסוים. רק כשחומר מגיע לסביבת הגידול, הטבעת משנה את מיקומה או מתפרקת, התרופה משתחררת בדיוק מרבי, ובמקביל החיישן "נדלק" ומדווח לרופאים "הגעתי למטרה והטיפול החל". כך, במקום לתת טיפול עיוור, הרופאים יכולים לראות איך התרופה פועלת בזמן אמת באמצעות MRI או מיקרוסקופיה פלואורסצנטית.
"אנחנו כמדענים צריכים להיות מולטי-טאסקינג", אומר ד"ר סעדי בחיוך, "והרוטקסן דומה לנו: יש לו פונקציות שונות שאפשר לשנות בו-זמנית, והוא עדיין מולקולה אחת". למשל, אפשר להנדס את הטבעת כך שתתפרק במקום שיש בו ריכוז גבוה של אנזים ספציפי לתאים סרטניים, או לחלופין בתנאי חומציות מסוימים – כמו אלה השוררים בקיבה. "אפשר לקחת פונקציה אחת ולגרום לה להיות ספציפית למטרה מסוימת", הוא מפרט. "כל שינוי כימי שאפשר לחשוב עליו אפשר להתאים לצרכים שלנו, וזה כולל גם רפואה מותאמת אישית בעתיד".
 המעבדה של ד"ר סעדי בבר-אילן. "אני חייב את השכנים שלי בביולוגיה ובפיזיקה וטוב שאנחנו נמצאים תחת קורת גג אחת".
המעבדה של ד"ר סעדי בבר-אילן. "אני חייב את השכנים שלי בביולוגיה ובפיזיקה וטוב שאנחנו נמצאים תחת קורת גג אחת".
פרשת התלידומיד: הכיוון המולקולרי שעושה את ההבדל
במסגרת הפוסט-דוקטורט של ד"ר סעדי באוניברסיטת סאות'המפטון ואוניברסיטת ברמינגהם באנגליה, תחת הנחייתו של ד"ר סטיב גולדאפ, ד"ר סעדי רכש ידע וניסיון בהכנה של רוטקסן כיראליים. מושג הכיראליות (מלשון "כף יד" ביוונית) מתאר מולקולות שהן תמונת ראי האחת של השנייה, בדומה לכפות הידיים שלנו. למרות שהן נראות זהות, הן אינן חופפות, והשפעתן על הגוף יכולה להיות הפוכה בתכלית. "הגוף הוא סביבה כיראלית – הוא יודע להבדיל בין מולקולה 'ימנית' ל'שמאלית'", הוא מסביר.
מכיוון שהתאים בגוף מגיבים אחרת לכל כיוון מולקולרי, היכולת לסנתז במעבדה מכונה בעלת כיווניות ספציפית היא קריטית ליעילות הטיפול ולבטיחות המטופל.
כדי להסביר את החשיבות הקריטית של הכיראליות, ד"ר סעדי חוזר לאחד האסונות התרופתיים הגדולים בהיסטוריה: פרשת התלידומיד. "התרופה פותחה בשנות החמישים בגרמניה כדי לטפל בנשים בהיריון שסבלו מבחילות בוקר", הוא מספר. "הבעיה הייתה שהתרופה הכילה תערובת של שתי המולקולות הכיראליות – תמונות הראי. בעוד צורון אחד אכן טיפל בבחילות, תמונת הראי שלו הייתה רעילה וגרמה לאסון עולמי: אלפי תינוקות מתו בלידה ורבים אחרים נולדו עם מומים קשים, ללא ידיים או רגליים".
הלקח הזה עומד בבסיס עבודתו. "במעבדה, האתגר הוא לייצר רק את הצורון ה'טוב' ולא את תמונת הראי שלו. היכולת לסנתז מכונה בעלת כיווניות ספציפית היא קריטית לבטיחות המטופל".
ד"ר סעדי משלב בעבודתו ניסיון עשיר בסינתזה יעילה, כפי שבא לידי ביטוי בפטנט הרשום שבו הוא מחזיק מתקופת הדוקטורט שבה עבד במעבדה של פרופ' בלהה פישר, חוקרת מובילה אחרת במרכז דנגור. מדובר בפיתוח שיטה סינתטית לייצור חומר פלואורסצנטי ייחודי לצביעת גרעינונים בתא – כלי אבחוני שכבר הפך למסחרי ומשרת מעבדות רבות בעולם ומבטיח דיוק מרבי בזיהוי תהליכים פתולוגיים.
הבית של המדע: שיתופי הפעולה במרכז דנגור
ד"ר סעדי מדגיש שוב ושוב כי המדע המודרני אינו עבודה של אדם בודד. "אני כימאי סינתטי, אני מתמחה בהכנת החומר", הוא אומר, "אבל כדי שהוא יעבוד אני חייב את השכנים שלי בביולוגיה ובפיזיקה וטוב שאנחנו נמצאים תחת קורת גג אחת". השהות במכון לננו-טכנולוגיה (BINA) ובמרכז דנגור מאפשרת לו שיח יומיומי עם חוקרים מתחומים שונים. "שיתופי הפעולה האלו, כולל עם היחידה לרפואה גרעינית בבית החולים שיבא, הם אלו שהופכים את המחקר מתיאורטי ליישומי".
ד"ר סעדי אינו מתעלם מהאתגרים. "אנחנו עדיין לא שם", הוא אומר בכנות. "יש לנו הוכחות שאפשר לבנות רוטקסנים ולפרק אותם באנזימים ספציפיים, אבל עכשיו אנחנו עובדים על אופטימיזציה של התהליך". האתגר הוא לא רק לייצר את המכונה המולקולרית, אלא גם לעשות זאת ביעילות גבוהה מספיק.
"בשנתיים האחרונות הצלחנו להכין שלושה חומרים שלא הוכנו מעולם, בדרכים שלא היו ידועות. אלו היו רגעים מרגשים מאוד, גם לי וגם לסטודנטים. אבל עכשיו אנחנו צריכים לשפר את היעילות – במקום מיליגרם בודד, לקבל כמות גדולה יותר שתאפשר לנו להתקדם לבדיקות הרצויות".
השימוש בסימולציות מחשב מתקדמות (Molecular Dynamics) מסייע לד"ר סעדי 'לצייר' את המכונות ולבדוק את היציבות שלהן עוד לפני שלב המבחנה. המחשב מריץ סימולציות 24 שעות ביממה, בודק ברמת דיוק של %95 אם המכונה תתפרק בדרך, וחוסך לחוקר ולתלמידיו זמן יקר מאוד, שמאפשר להם להתקדם במחקר במהירות.
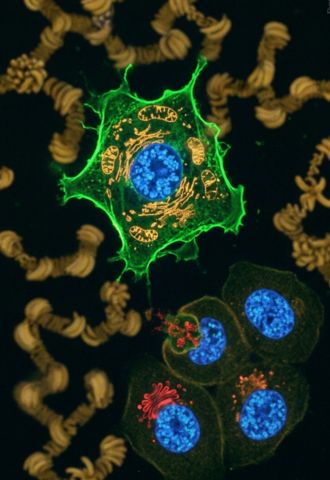 ייצור חומר פלואורסצנטי ייחודי לצביעת גרעינונים בתא – כלי אבחוני שהפך למסחרי, משרת מעבדות רבות בעולם ומבטיח דיוק מרבי בזיהוי תהליכים פתולוגיים.
ייצור חומר פלואורסצנטי ייחודי לצביעת גרעינונים בתא – כלי אבחוני שהפך למסחרי, משרת מעבדות רבות בעולם ומבטיח דיוק מרבי בזיהוי תהליכים פתולוגיים.
חוקר ערבי-ישראלי בזמן מלחמה: אי של שפיות
ד"ר סעדי מייצג את חוד החנית של דור החוקרים הצעיר שצמח באוניברסיטת בר-אילן, שבה השלים את כל תאריו בהצטיינות יתרה. החזרה שלו למחלקה כחבר סגל בכיר ב-2024 הייתה מרגשת במיוחד: " זה הרגיש כמו לחזור הביתה".
החזרה הביתה הייתה גם החזרה למשפחה. לד"ר סעדי שני ילדים – בן ובת – והבן בן השבע מלווה אותו לאוניברסיטה בחופשות. חזרתו לישראל מאנגליה בעיצומה של המלחמה, ביוני 2024, לא הייתה מובנת מאליה. "למרות החששות הטבעיים, כחוקר ערבי-ישראלי לא הרגשתי שום שינוי ביחס אליי בבר-אילן. כולם קיבלו אותי בזרועות פתוחות". סעדי, שהחליט מראש להתנתק מפוליטיקה ולהתמקד במדע, לא נתן לדברים האלה להשפיע עליו. "אני איש מדע, זה מה שמעניין אותי", הוא אומר בשלווה. "פוליטיקה אני משאיר לאנשי הפוליטיקה".
 ד"ר עבד סעדי: הצלחנו להכין דברים שהרגישו בלתי אפשריים. זה לא מתבשל בן-לילה – פיתוח תרופה לוקח בין 10 ל-20 שנה.
ד"ר עבד סעדי: הצלחנו להכין דברים שהרגישו בלתי אפשריים. זה לא מתבשל בן-לילה – פיתוח תרופה לוקח בין 10 ל-20 שנה.
חזון לעשור הבא: רפואה תפורה אישית לכל חולה
כשהוא נשאל על העתיד, סעדי מדבר על רפואה מותאמת אישית. "אנחנו שואפים למקום שבו לא ניתן טיפול 'ממוצע' לכולם, אלא נתכנן רוטקסן שנתפר במעבדה בדיוק לפי המאפיינים המולקולריים של חולה ספציפי כך שהטיפול יהיה יעיל ומדויק יותר מאי פעם. הטבע עושה את זה בשיעורי הצלחה של מאה אחוזים – הריבוזום שלנו הוא המכונה המושלמת. אנחנו לא מתחרים בטבע, אנחנו לומדים ממנו".
הדרך לפריצת דרך מדעית אינה קלה. "לפעמים אתה מתכנן חומר שלא היה קיים מעולם, ואתה בטוח שזה יעבוד", משתף ד"ר סעדי, "ואז אתה מנסה פעם אחר פעם אחר פעם, ולא מצליח". בניגוד לתדמית הרומנטית של המדען הבודד שעובד במעבדתו, הוא מדגיש את חשיבות העבודה הקבוצתית: "יחד עם הסטודנטים המוכשרים שלי הצלחנו להכין דברים שהרגישו בלתי אפשריים. זה לא מתבשל בן-לילה – פיתוח תרופה לוקח בין 10 ל-20 שנה".
ד"ר סעדי רואה את תפקידו כמנחה כלא פחות חשוב מהמחקר עצמו: "הדבר הכי חשוב הוא לגדל דור שאכפת לו מהמדע. סטודנטים שקמים בבוקר ובאים למעבדה כי הם אוהבים את מה שהם עושים. בשנים האחרונות יש ירידה משמעותית במספר הסטודנטים שרוצים להמשיך לתארים מתקדמים, והמשאב הזה – של אנשים סקרנים ומסורים – הוא הכי גדול שיש לנו. רעיונות טובים לבד לא יספיקו אם אין מי שיוציא אותם לפועל".
מאז הקמת המעבדה באוקטובר 2024, הצליח ד"ר סעדי לגייס שמונה עמיתי מחקר, שכוללים פוסט-דוקטורנטים, דוקטורנטים וסטודנטים לתואר שני ועובדים במעבדה, וארבעה מאמרים מדעיים כבר פורסמו. "אני מאוד גאה בזה", הוא אומר, "אבל אנחנו עדיין בשלב הפיתוח. האפליקציות המעשיות יבואו בהמשך".
סעדי, שמקדיש שעות ארוכות למדע, רואה בעבודתו שליחות: "החלום שלי הוא להביא מוצר יישומי לשוק התרופות. עד אז, אני מתמקד בגידול דור חדש של מדענים סקרנים, כאלו שמבינים שכימיה היא הדרך שלנו לבנות עולם טוב יותר".
תאריך עדכון אחרון : 27/04/2026