תהליכי הזדקנות: האם הפתרון למחלה נדירה יאט את הזקנה של כולנו?

במשך שנים, אנשים צעירים שהחלו להראות סימני זקנה מואצים נחשבו לחולי אלצהיימר או פרקינסון. ריאיון עם ד"ר רונית אילוז, ממרכז דנגור לרפואה מותאמת אישית באוניברסיטת בר־אילן, מלמד על מחקר פורץ דרך שחשף מחלה חדשה. הגילוי עשוי להעניק מפתח לעצירת הידרדרות המוח לא רק אצל חולים נדירים, אלא גם אצל כל אחד מאיתנו
במרכז המעבדה של ד"ר רונית אילוז באוניברסיטת בר-אילן עומד אנזים אחד קריטי בשם PKA והוא המנצח על התזמורת: הוא מפעיל ומווסת את הפעילות העצבית במוח ושולט על העברת המסרים. "הוא מקבל החלטות עבור תא העצב: איך לעבוד, ואיך להעביר מסרים", מסבירה אילוז.
ל-PKA יש "אחים" – גרסאות שונות של אותו חלבון שנקראות איזופורמים. "כמו משפחה שבה כל האחים דומים מאוד במבנה שלהם, אבל לכל אחד אישיות ותפקיד שונה לחלוטין", היא מוסיפה, "אנחנו חוקרים איזופורם ספציפי שנמצא בריכוז גבוה מאוד במוח, שנקרא R1β) R1-beta). השאלה ששאלנו היא מה התפקיד שלו, ומה קורה כשהוא פגום".
המעבדה כ"מפת גוגל" לחלבונים
ד"ר אילוז היא מומחית עולמית בארגון התאי של חלבוני איתות - חלבונים חיוניים המתווכים תקשורת בין תאים, פועלים כ"שליחים" המעבירים מידע מחוץ לתא פנימה, ומפעילים שרשרת תגובות כימיות להשפעה על תפקוד התא, כמו גדילה, התמיינות, חלוקה או תגובה לגירויים. הקריירה שלה הוקדשה להבנת המנגנונים הללו – מהדוקטורט בגנטיקה וביוכימיה באוניברסיטת תל אביב ועד לפוסט-דוקטורט היוקרתי במכון הרפואי HHMI באוניבריטת קליפורניה שבסן דייגו בארה"ב. העבודה שלה נראית לעיתים כמו עבודת בילוש מולקולרית: היא הצליחה לפענח את המבנה התלת-ממדי של האנזים ומשם היא בוחנת מה השתבש במחלה.
החידוש המרכזי של ד"ר אילוז טמון בהבנה שביולוגיה היא לא רק "מה" אלא בעיקר "איפה". היא פיתחה טכנולוגיית מיפוי ברזולוציה גבוהה – מעין "מפת גוגל" לחלבוני איתות – המאפשרת לראות את המיקום המדויק (לוקליזציה) של כל חלבון בתוך האברונים התאיים.
"לכל אנזים יש חלק שמפעיל אותו וחלק מעכב. בעזרת פיצוח המבנה התלת-ממדי של החלבון הצלחנו לזהות ולהבין מהם החלקים השונים והקשרים ביניהם. חלבון חייב לעבוד במקום הנכון ובזמן הנכון. אם נבין את המיקום והתזמון, נוכל לשלוט בעיכוב או בהאצה שלהם", היא אומרת. "במעבדה אנחנו בודקים איך היחידה הפעילה של האנזים עוברת עיכוב. זה קריטי, כי כשהיא פעילה מדי זה לא טוב, וכשהיא מעוכבת מדי – המחלה מתפרצת. בזכות המפה הזו אנחנו יכולים להבין איך לשלוט בעיכוב או בהאצה שלהם ומשם הדרך לטיפול תרופתי מאזן מתקצרת".
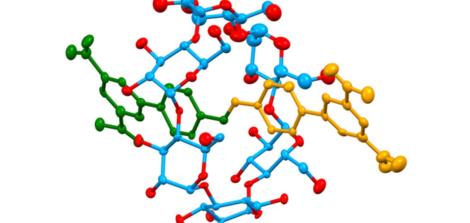
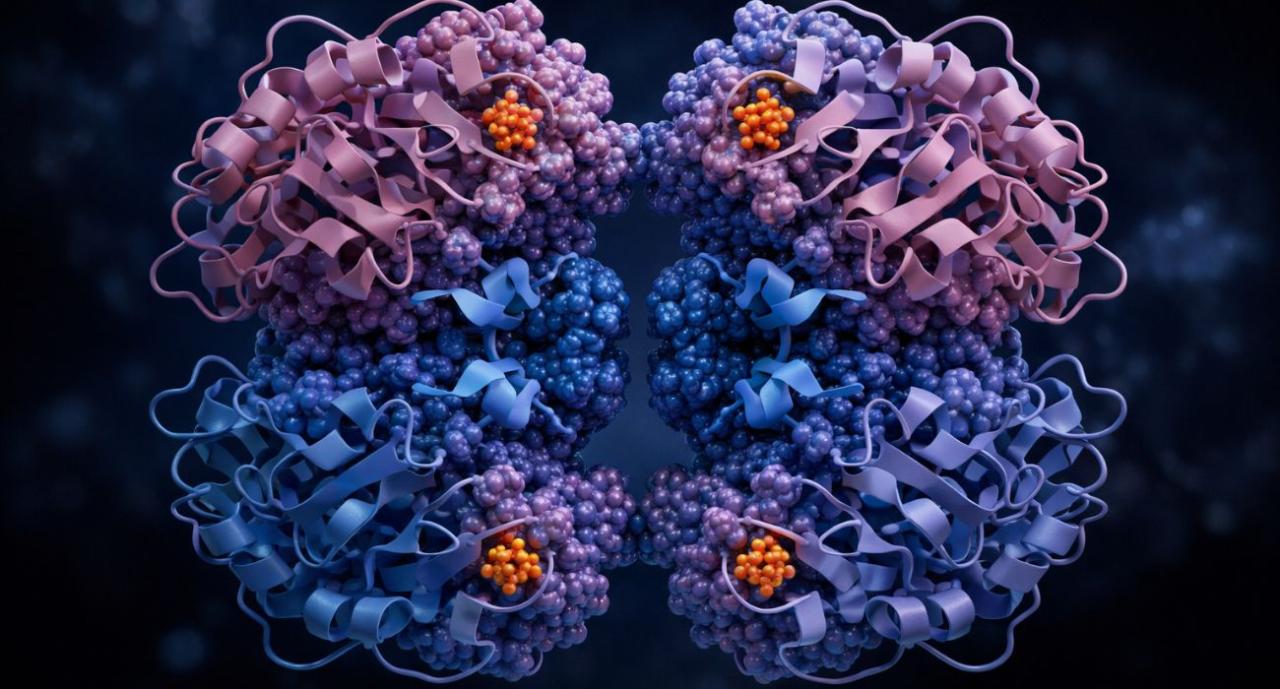 מודל תלת־ממדי של PKA
מודל תלת־ממדי של PKA
התעלומה ההולנדית ושיתוף הפעולה הדו-לאומי
המחקר במעבדה של אילוז קיבל תפנית דרמטית כשקבוצת רופאים מהולנד זיהתה משפחה הסובלת מתסמינים נוירודגנרטיביים מסתוריים העוברים בתורשה. "הם מצאו מוטציות גנטיות ספציפיות ב-R1β, היחידה הרגולטורית שמעכבת את האנזים", משחזרת ד"ר אילוז. חמושה במבנה התלת-ממדי שפענחה היא ניגשה להבין את המוטציה: "האינטראקציה בין היחידות שמרכיבות את האנזים צריכה להיות כמו כפפה ליד, והמוטציה הזו פשוט 'דוחפת' את החלקים ולא מאפשרת להם להתחבר".
הטרגדיה היא העיתוי שבו התהליכים מתרחשים. "גילינו שהמוטציה הזו פשוט מזרזת תהליכי הזדקנות שקורים ממילא לכולנו בגיל מבוגר, אבל אצל החולים האלו – הכול מואץ כבר בגיל 45", מתארת אילוז ומפרטת: "אנשים צעירים מתחילים להראות סימני זקנה מואצים – הזיכרון נחלש, הלימוד הופך איטי, וצריך מאמץ כדי לשלוף מידע פשוט כמו 'איפה המפתחות?'"
התסמינים של המחלה החדשה שד"ר אילוז הגדירה, NLPD-PKA, כוללים בעיות מוטוריות קשות, הליכה שפופה ופגיעה בזיכרון. כדי לחקור אותה, ד"ר אילוז חקרה מוחות של נפטרים שהגיעו אליה מהולנד, לצד יצירת עכברי מודל עם המוטציה האנושית. "מדהים עד כמה המוח של העכבר דומה לזה של האדם. אנחנו מזריקים להם חומרים שמעוררים פעילות כדי לראות איך המוח מתנהג במצב נייח לעומת מצב פעיל".
זיהוי המחלה החדשה והתובנות להמשך עבודה זיכו לאחרונה את ד"ר אילוז במענק מחקר יוקרתי מהקרן הדו-לאומית ישראל-ארה"ב (BSF), בשיתוף פעולה עם ד"ר רודריגו מיילארד מאוניברסיטת ג'ורג'טאון. יחד, שתי המעבדות משלבות מומחיות כדי לפצח את המנגנונים המולקולריים המובילים להזדקנות המואצת.
המחלה שמאיצה את הזמן: פוטנציאל עצום לטיפול בזקנה
אחד הממצאים המטלטלים במחקר הוא הקשר להזדקנות הכללית. "ראינו שכל התסמינים שאנחנו מוצאים בעכברים החולים קורים ממילא עם הזמן גם במצב הבריא".
כאן נכנסת הרפואה המותאמת אישית של מרכז דנגור לתמונה. כיום ידועים רק כ-12 חולים מאובחנים בעולם שעברו ריצוף גנטי מלא. המחלה אולי נדירה, אך הפוטנציאל שלה עצום. חברות התרופות הגדולות לרוב נרתעות מהשקעה במחלות יתומות מסיבות כלכליות, אך כאן המקרה שונה.
"לחקור זקנה זה 'גדול' מדי, יש יותר מדי תהליכים", מסבירה ד"ר אילוז, "אבל כשיש לנו מחלה שנובעת מפגיעה באנזים ספציפי, יש לנו עוגן. אם נלמד לתקן את ה-RIβ אצל החולים הללו, נוכל להשליך מכך על כולנו. הפתרון למחלה הנדירה עשוי להיות הטיפול שיאט את הזקנה של האוכלוסייה כולה".
המחקר כבר מראה פוטנציאל מעבר לחקר המוח: ד"ר אילוז מיישמת את תובנות ה-PKA גם בחקר סרטן הערמונית, שם היא עובדת בשיתוף פעולה הדוק עם רופאים וחולים. "הקשר בין הקליניקה למעבדה הוא קריטי", היא מסבירה. "המידע שאני מקבלת מפציינטים משפיע ישירות על מה שאנחנו עושים במעבדה".
מדע בצל המלחמה: "הערות לא מדעיות"
כחוקרת שהקימה והובילה את מרכז ScienceAbroad בסן דייגו, ד"ר אילוז רגישה למעמדו של המדע הישראלי. כיום, היא חשה את אתגרי השלכות המלחמה בזירה האקדמית. "היה לי מאמר שנדחה, וכשקראתי את הערות הסוקרים זה היה פשוט הזוי. זה לא היה מדעי", היא מספרת בכנות. "הסברתי להם דברים פשוטים שהם פשוט 'לא הבינו' כביכול. קשה שלא לחשוב על אנטישמיות כשלא מוצאים שום עילה מדעית אחרת לפסילת עבודה".
למרות זאת, היא ממשיכה להציג את עבודתה בכנסים בינלאומיים, שם חוקרים מתרגשים מהגישה האינטרדיסציפלינרית שלה החולשת על תחומי הביוכימיה, הגנטיקה, המבנה והמיקרוסקופיה המתקדמת. "הרבה פעמים אנשים חוקרים רק תחום אחד, ואין להם את התמונה הרחבה. בלי התמונה הזו, הרבה יותר קשה לדייק את הדרך לפתרון".
החזון: לחיות בכבוד
בעתיד, ד"ר אילוז שואפת להמשיך ולפצח את המנעד כולו: ממחלות נדירות שמביאות לבעיות התפתחותיות בילדים, דרך בעיות נוירולוגיות שמביאות למחלות נוירודגנרטיביות ועד לזקנה עצמה. "הכול קשור זה לזה", אומרת אילוז. "הכי מעניין אותי להגיע לפתרון שיהפוך את המחלות הקשות האלו למשהו שאפשר לחיות איתו בכבוד".
הסקרנות, היא מסכמת, היא המניע למחקר שלה. "הכי מרגש אותי למצוא תשובה, וכל תשובה מביאה לעוד עשר שאלות חדשות. לראות איפה היינו לפני ארבע שנים עם ההשערות שהיו לנו, ומה אנחנו מגלים היום, לאן פרצנו? זו דרך מופלאה ממש".
 ד"ר רונית אילוז במעבדה, מרכז דנגור, אוניברסיטת בר-אילן
ד"ר רונית אילוז במעבדה, מרכז דנגור, אוניברסיטת בר-אילן
תאריך עדכון אחרון : 02/03/2026